Hvilke nye behandlinger av glioblastom planlegges utprøvd?
Det helsevitenskapelig fakultet, UiT – Norges arktiske universitet
Institutt for klinisk medisin, Det helsevitenskapelig fakultet, UiT – Norges arktiske universitet og Hjerte- og lungeklinikken, Universitetssykehuset Nord-Norge, Tromsø
Institutt for klinisk medisin, Det helsevitenskapelig fakultet, UiT – Norges arktiske universitet og Nevro-, ortopedi- og rehabiliteringsklinikken, Universitetssykehuset Nord-Norge, Tromsø.
Sammendrag
Bakgrunn
Glioblastom er en hjernekreftsykdom som med dagens standard behandling har dårlig prognose. Målet med denne undersøkelsen var å kartlegge hvilke kliniske studier av nye behandlinger som planlegges eller er i oppstartsfase.
Materiale og metode
Vi gjorde en tverrsnittsundersøkelse av planlagte studier registrert i databasen ClinicalTrials.gov. Kliniske studier av aktive behandlingstiltak ble inkludert.
Resultater
Det var pr. 8.1.2020 registrert 45 planlagte studier hvorav 16 skal undersøke effekten av ny antineoplastisk behandling, elleve av immunterapi, fem av strålebehandling, og åtte av kombinasjon av to eller flere av disse behandlingsformene. Det er planlagt flest studier av nåværende standard antineoplastiske behandling (temozolomid) kombinert med andre medikamenter (n=9) og av immun-sjekkpunkthemmere (n=6). De fleste er fase 1 eller 2-studier.
Fortolkning
Cytostatika, andre antineoplastiske medikamenter og immunterapi er prioriterte forskningsfelt i behandlingen av glioblastom. Immunterapi har revolusjonert behandlingen av andre kreftsykdommer, men det er planlagt få nye fase 3-studier av slik behandling ved glioblastom.

Illustrasjonsfoto: Colourbox
Bakgrunn
Glioblastom er en alvorlig intrakranial kreftsykdom. Insidensen øker med alderen og sykdommen rammer omtrent 230 norske pasienter i året. Median alder ved diagnosetidspunktet er 62 år, og gjennomsnittlig levetid ni måneder (1). Standard behandling er kirurgisk reseksjon og postoperativ cellegiftbehandling med temolozomid som gis både konkomitant og adjuvant til strålebehandling (2).
Det er et helsepolitisk mål å tilby flere kreftpasienter med dårlig prognose utprøvende behandling gjennom inklusjon i kliniske studier. Det pågår pr. januar 2021 ingen aktive fase 3- eller 4-studier av behandling av ny-diagnostisert glioblastom i Norge. Pasientene har dermed begrensede muligheter for å delta i utprøvende behandling. Målet med denne undersøkelsen var derfor å kartlegge hvor mange kliniske studier av nye behandlinger som planlegges eller er i oppstartsfase.
Materiale og metode
ClinicalTrials.gov er en database som drives av National Institutes of Health i USA (3). Registrering av studier som medfører utprøving av nye medikamenter eller andre intervensjoner er obligatorisk i USA, Norge og de fleste andre vestlige land.
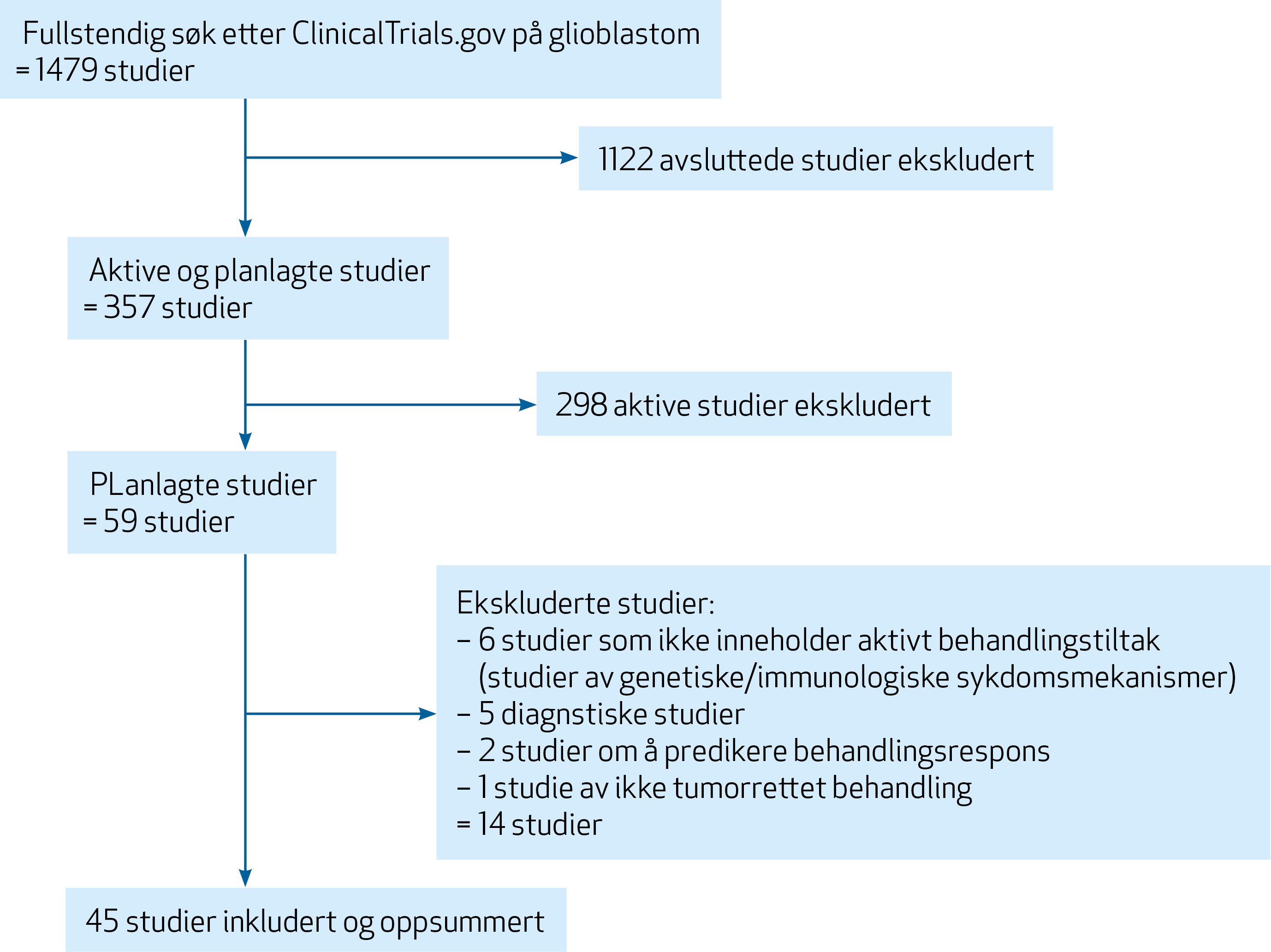
Figur 1. Flytskjema som viser prosessen for inklusjon og eksklusjon av studier.
Vi gjennomførte et søk som identifiserte alle studier av glioblastom registrert hos ClinicalTrials.gov pr. 8. januar 2020. Figur 1 over viser at vi inkluderte alle planlagte studier av aktive behandlingstiltak som ennå ikke hadde startet pasientinklusjon. Avsluttede studier, studier med pågående pasientinklusjon, studier som ikke evaluerte effekt av aktiv tumorrettet behandling, studier av diagnostiske metoder og studier med målsetting om å predikere behandlingsrespons for allerede etablerte behandlingsformer ble ekskludert. Faktaboksen under viser definisjoner av studiefaser.
Definisjon av studiefaser
Fase 1-studie
Undersøkelse av medikamentets farmakokinetikk, interaksjoner og dosering hos friske frivillige forsøkspersoner.
Fase 2-studie
Undersøkelse av behandlingseffekt ved forskjellige doseringer hos et mindre antall pasienter.
Fase 3-studie
Studier av behandlingseffekt og sikkerhet hos en større pasientgruppe, og sammenligning med kontroller (randomisert forsøk). Nødvendig for markedsføringstillatelse.
Fase 4-studie
Studier som undersøker behandlingseffekt hos store pasientgrupper etter at medikamentet er godkjent og i rutinemessig bruk.
Resultater
Blant de 45 inkluderte studiene skal 16 omhandle antineoplastisk behandling, elleve immunterapi, fem strålebehandling, åtte kombinasjon av to eller flere av disse behandlingene og fem andre behandlingsformer. Tabell 1 under viser at det planlegges flest fase 1-studier, litt færre fase 2-studier, men ingen rene fase 3-eller 4-studier. Ti studier er registrert som kombinasjon av fase 1 og 2, og to som kombinasjon av fase 2 og 3.
Antall studier |
|||||||
|---|---|---|---|---|---|---|---|
Intervensjon |
Totalt |
Fase 1 |
Fase 2 |
Fase 1+2 |
Fase 3 |
Fase 2+3 |
Ikke oppgitt |
Antineoplastiske medikamenter |
16 |
6 |
2 |
6 |
1 |
1 |
|
Immunterapi |
11 |
4 |
4 |
2 |
1 |
||
Stråleterapi |
5 |
1 |
2 |
2 |
|||
Annet |
5 |
4 |
1 |
||||
Kombinasjon |
8 |
5 |
2 |
1 |
|||
Totalt |
45 |
16 |
14 |
10 |
0 |
2 |
3 |
Antineoplastisk behandling
I kategorien antineoplastiske medikamenter planlegges 16 studier. Medikamenter som cytostatika, intracellulære signalhemmere, angiogenesehemmere, medikamenter som induserer autofagi og stråle- samt cytostatikasensitiserende medikamenter er definert som antineoplastisk behandling.
Ni av de 16 studiene skal undersøke effekten av dagens standardbehandling kombinert med et annet medikament. Flere av medikamentene er godkjent for bruk ved andre sykdommer (såkalt «re-purposing»), eksempelvis klorokin i malariabehandling og levetiracetam mot epilepsi. Tre studier skal undersøke kombinasjonen av temozolomid og cannabidiol, og en kombinasjonen av temozolomid og protein kinase C-hemmeren enzastaurin. Prekliniske studier har vist at enzastaurin har cytotoksisk effekt mot glioblastom-cellene ved å hemme angiogenesen (4). Tyrosin kinasehemmeren anlotinib hemmer angiogenese og cellevekst, og skal i en studie undersøkes i kombinasjon med temozolomid (5). En studie skal undersøke om antisekretorisk faktor øker opptaket av temozolomid i tumorceller og dermed gir økt behandlingseffekt (6).
Det planlegges fire studier som skal undersøke effekten av angiogenesehemmeren bevacizumab kombinert med andre monoklonale antistoffer og immunsjekkpunkthemmere. En femte studie skal undersøke kombinasjonen av bevacizumab og en matrix metalloproteina se 9 (MMP9)-hemmer. MMP9 er en endopeptidase som remodellerer ekstracellulær matriks ved å kløyve viktige strukturelle elementer (7).
To studier skal undersøke om andre antineoplastiske medikamenter kan gi bedre effekt enn temozolomid. ABM-1310 inhiberer cellesignalproteinet RAF og OKN-007 reduserer kreftcellenes angiogenese og stimulerer apoptose (8, 9).
Illustrasjonsfoto: Colourbox
Immunterapi
Glioblastomers mikromiljøer ser ut til å være sterkt immunosuppressive. Immunterapi innbefatter et stort spekter av medikamenter som søker å forsterke immunresponsen mot tumor. Seks studier skal undersøke effekten av immun-sjekkpunkthemmerne pembrolizumab og atezolizumab kombinert med andre antistoffer (10). Fire studier skal undersøke effekten av pembrolizumab og to effekten av atezolizumab, i kombinasjon med antineoplastiske medikamenter og/eller kreftvaksiner, hvorav to administreres intratumoralt.
En studie skal undersøke effekten av ipilimumab og nivolumab, som i dag er godkjent for behandling av metastaserende malignt melanom. En studie skal undersøke effekten av virusterapi ved å injisere et genmodifisert virus i tumor for å initiere en immunrespons. Tre studier skal undersøke T-celleterapi, og to kreftvaksiner.
Strålebehandling
Det er planlagt fem studier som skal undersøke effekten av nye stråleregimer. En skal studere effekten av ny strålebehandling ved tilbakefall og en annen effekten av hypofraksjonert bestråling. Det er også planlagt to studier av preoperativ bestråling og to av behandling med alternerende elektriske felt med middels frekvens og lav intensitet (eng. tumor treating fields (TTF)).
Tre studier skal kombinere henholdsvis stereotaktisk bestråling eller hypofraksjonert bestråling med immun-sjekkpunkthemmere. En studie skal undersøke effekten av TTF kombinert med betablokkeren carvedilol, og en annen studie skal se på effekten av stråleterapi kombinert med det antineoplastiske medikamentet CAN-008.
Annet
Det planlegges en studie som skal undersøke om nye MR-metoder kan muliggjøre bedre tumorreseksjon, en som skal studere effekten av fotodynamisk terapi, en som skal undersøke effekten av et strålesensitiserende medikament og en som skal undersøke effekten av et medikament som har redusert behandlingsresistens i dyremodeller.
Diskusjon
Denne gjennomgangen av planlagte studier viser at cytostatika, andre antineoplastiske medikamenter og immunterapi er prioriterte forskningsfelt i behandlingen av glioblastom. To tredjedeler av studiene skal undersøke ny behandling i kombinasjon med allerede etablert behandling og en tredjedel moderne immunterapi. Studier av temozolomid i kombinasjon med andre medikamenter, eller bruk av immunsjekkpunkthemmere i tillegg til standard behandling dominerer.
Innen immunterapi ved glioblastom er det planlagt flest studier av behandling med monoklonale antistoffer, herunder immun-sjekkpunkthemmere. Disse har revolusjonert behandlingen av andre kreftformer.
Vår gjennomgang viser imidlertid at det er planlagt få fase 3-studier. Det skyldes sannsynligvis at mange medikamenter og intervensjoner som undersøkes i fase 1 og 2 ikke har ønsket effekt, eller viser en uakseptabel bivirkningsprofil. Hvis det vedvarer, vil kirurgisk reseksjon kombinert med temozolomid og strålebehandling forbli beste behandling, til tross for utilfredsstillende behandlingsresultater.
Det er en svakhet at vi har gjennomført en tverrsnittsundersøkelse, og dermed ikke kan presentere et helhetlig dynamisk bilde av hvor mange tidligfasestudier som går videre til fase 3. En fullstendig oversikt krever longitudinelt studiedesign. Vi har heller ikke gjennomgått detaljerte protokoller for de inkluderte studiene. Dette medfører noe risiko for å overse vesentlig informasjon.
Det er et politisk mål i Norge at en større andel pasienter med alvorlig kreftsykdom skal tilbys utprøvende behandling. Helseforetakene er i oppdragsdokumentene bedt om å legge til rette for dette. Denne gjennomgangen viser imidlertid at det er planlagt få studier som vil bli aktuelle for denne pasientgruppen. Det kan tolkes i retning av at tradisjonelle randomiserte kontrollerte kliniske forsøk gir lite håp for pasienter med glioblastom.
Persontilpasset behandling basert på genomikk, dyrking av tumorsfærer og in vitro screening av et stort antall medikamenters effekt på den enkelte tumor, er en ny og alternativ tilnærming. Ved «re-purposing» (ny bruk av gamle medikamenter) kan man korte ned utviklingstiden fordi fase 1-studier er gjennomført fra før. Det er planlagt større nasjonale forskningsprosjekter for utprøving av en slik tilnærming i Norge (11).
Hovedfunn
Det er registrert 45 planlagte studier av ny behandling mot glioblastom på ClinicalTrials.gov. To tredjedeler av studiene skal undersøke kombinasjoner av allerede etablert og ny behandling, og en tredjedel ny moderne immunterapi.
Referanser
Storstein A, Helseth E, Johannesen T.B. et al. Høygradige gliomer hos voksne. Tidsskr Nor Legeforen 2011; 3: 238-41.
Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av diffuse høygradige gliomer hos voksne. Rapport IS-2936. Oslo: Helsedirektoratet 2020. https://www.helsedirektoratet.no/retningslinjer/hjernesvulster-handlingsprogram. Lest 21.12.2020.
ClinicalTrials.gov: National Library of Medicine. https://clinicaltrials.gov/ct2/about-site/backround. Lest 21.1.2020.
Kreisl TN, Kotliarova S, Butman JA et al. A phase I/II trial of enzastaurin in patients with recurrent high-grade gliomas. Neuro Oncol 2010; 12:181-9.
Lv Y, Zhang J, Liu F et al. Targeted therapy with anlotinib for patient with recurrent glioblastoma: A case report and literature review. Medicine (Baltimore) 2019; 98: e15749.
Ilkhanizadeh S, Sabelström H, Miroshnikova YA et al. Antisecretory factor–mediated inhibition of cell volume dynamics produces antitumor activity in glioblastoma. Mol Cancer Res 2018; 16: 777-90.
Tabouret E, Boudouresque F, Farina P et al. MMP2 and MMP9 as candidate biomarkers to monitor bevacizumab therapy in high-grade glioma. Neuro Oncol 2015; 17: 1174-6.
Zhao C. Safety of ABM-1310 monotherapy in patients with advanced solid tumors. ClinicalTrials.gov. https://clinicaltrials.gov/ct2/show/NCT04190628. Lest 21.1.2020.
Towner RA, Smith N, Saunders D et al. OKN-007 Increases temozolomide (TMZ) sensitivity and suppresses TMZ-resistant llioblastoma (GBM) tumor growth. Transl Oncol 2019; 12: 320-35.
Weller M, Le Rhun E. Immunotherapy for glioblastoma: quo vadis? Nat Rev Clin Oncol 2019; 16: 405-6.
Oslo universitetssykehus. IMPRESS-Norway. https://oslo-universitetssykehus.no/om-oss/nyheter/stor-nasjonal-presisjonsmedisinstudie-innen-kreft Lest 7.12.2020